Die Existenz diskreter Energiezustände für Elektronen in einem Atom, die wir erst im Bohrschen Atommodell kennenlernen, wird hier auch verwendet.
Bei dieser Ableitung werden wir auf Einsteins Photonenhypothese und das Bohrsche Atommodell vorgreifen. Einsteins Photonenhypothese ist die Annahme, dass Licht aus Teilchen besteht, den sogenannten Lichtquanten oder Photonen. Jedes Photon besitze die Energie ![]() .
.
Die Existenz diskreter Energiezustände für Elektronen in einem Atom, die wir erst im Bohrschen Atommodell kennenlernen, wird hier auch verwendet.
Wir betrachten zwei Energieniveaus in einem Atom, die sich um
einen Energiebetrag ![]() unterscheiden, und zwar:
unterscheiden, und zwar:
![]()
Zwischen zwei solchen Energieniveaus sind nach Einstein drei verschiedene Arten von Strahlungsübergängen möglich:
Im Bild unten werden diese Prozesse schematisch illustriert:
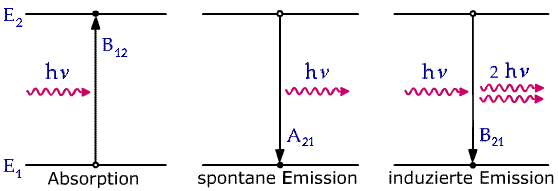
Nun betrachten wir ein System von N
Atomen in einem schwarzen Körper. Die Anzahl der Elektronen im Zustand
E 1
sei N1
und die Anzahl der Elektronen im Zustand E 2
sei N2. Die
Zahl N1 bzw.
N2 nennen
wir im Folgenden die Besetzungszahl des Zustands E 1
bzw. E 2.
Als Teil eines schwarzen Körpers steht das System im Gleichgewicht mit
einem elektromagnetischen Feld der Energiedichte u(![]() ).
Deswegen erfolgen gleich viele Elektronenübergänge von E 1
nach E 2
wie von E 2
nach E 1
pro Zeiteinheit:
).
Deswegen erfolgen gleich viele Elektronenübergänge von E 1
nach E 2
wie von E 2
nach E 1
pro Zeiteinheit:
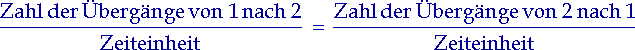
| (2.1) |
Diese Prozesse können mathematisch beschrieben werden:
Übergänge von 1 nach 2: Absorptionen:
Die Zahl der Übergänge von 1 nach 2 pro Zeiteinheit ist der Energiedichte u(![]() ) und der Besetzungszahl N1 proportional:
) und der Besetzungszahl N1 proportional:
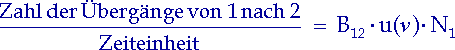
| (2.2) |
Der Proportionalitätsfaktor B12 heißt Einstein-Koeffizient. Er zeigt die Wahrscheinlichkeit eines Übergangs pro Zeit- und Energiedichte-Einheit an.
Übergänge von 2 nach 1: Spontane Emissionen und Induzierte Emissionen:
Die Zahl der Übergänge von 2 nach 1 pro Zeiteinheit setzt sich aus zwei Termen zusammen:
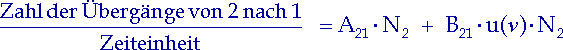
| (2.3) |
Der erste Term: A21 ![]() N2 ist die Zahl spontaner Emissionen und
N2 ist die Zahl spontaner Emissionen und
der zweite Term: B21 ![]() u(
u(![]() )
) ![]() N2 ist die Zahl induzierter Emissionen je Zeiteinheit.
N2 ist die Zahl induzierter Emissionen je Zeiteinheit.
A21 und B21 sind ebenfalls Einstein-Koeffizienten.
Wegen (2.1) (thermisches Gleichgewicht) ist die Zahl der Absorptionen gleich der Zahl der Emissionen:
| (2.4) |
Wir lösen diese Gleichung nach dem Verhältnis der Besetzungszahlen auf:
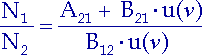
| (2.5) |
In der statistischen Thermodynamik wird die Verteilung der Teilchen des Gesamtsystems auf die verschiedenen möglichen Energieniveaus mit Hilfe der Boltzmann-Verteilungsfunktion beschrieben, so dass gilt:
Im thermischen Gleichgewicht verhalten sich die Besetzungszahlen N1 und N2 zueinander wie ![]() zu
zu ![]() :
:
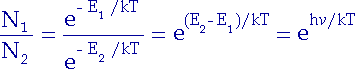
| (2.6) |
Gleichsetzen von (2.5) und (2.6) führt zu
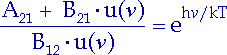
| (2.7) |
und Auflösen nach u(![]() ) zu
) zu
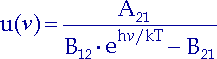
| (2.8) |
Für ![]() muss auch die Energiedichte beliebig groß werden: u(
muss auch die Energiedichte beliebig groß werden: u(![]() )
) ![]() .
.
Der Einsteinkoeffizient A21
ist endlich, deswegen wird der Nenner in (2.8)
gegen Null gehen:
| 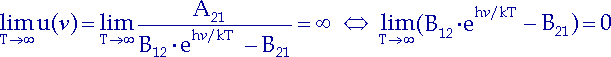
|
und wegen |
folgt: | (2.9) |
Diese Erkenntnis wenden wir in (2.8) an:
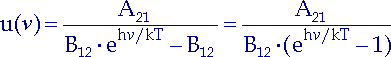
| (2.10) |
Das Verhältnis der verbleibenden Einsteinkoeffizienten erhalten wir durch Vergleich dieser Formel bei sehr kleinen Frequenzen mit dem Rayleigh-Jeans-Gesetz.
Mit der Reihenentwicklung | 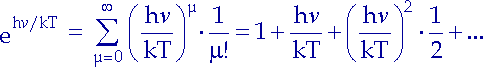
|
können wir für sehr kleine Frequenzen alle Summanden nach ![]() /kT vernachlässigen:
/kT vernachlässigen:
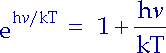
|
Das setzen wir in (2.10) ein: | 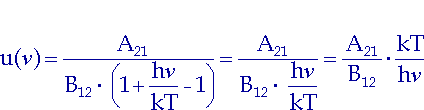
| (2.11) |
Nach Vergleich dieser Formel mit dem Rayleigh-Jeans-Gesetz: | 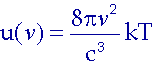
|
ergibt sich | 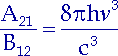
| (2.12) |
und schließlich die Plancksche Strahlungsformel:
Plancksche Strahlungformel | 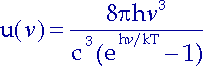
|
Einstein hat mit seiner Herleitung der Planckschen Strahlungsformel
einen sehr starken Hinweis für die Existenz der Quanten der Energie ![]() gegeben.
gegeben.