1. Aufgabe:
|
| Man betrachtet einen vollkommen elastischen runden Luftballon der auf Seehöhe losgelassen wird. Dort
herrscht ein Druck von 1013 mbar. Sein Durchmesser beträgt 5cm
(das Volumen einer Kugel berechnet sich aus: V = 4/3 p * r3).
Wie groß ist der Durchmesser des Ballons, wenn der Ballon aufsteigt und dabei der Druck auf 267,5
mbar sinkt?
Tip Antwort |
2. Aufgabe:
|
| Man betrachtet in Wasser gelöste Kohlensäure (H2CO3) in einer Minderalwasserflasche:
Die Kohlensäure darin zerfällt zu Wasser (H2O) und Kohlendioxid (CO2):
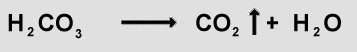
| (32) |
Das Volumen des entstehenden Kohlendioxids beträgt 15 cm3. Es herrscht eine Temperatur
von 5�C und der
Druck liegt bei 1525 mbar, da die Flasche im Kühlschrank steht und verschlossen ist.
Welches Volumen hat das Kohlendioxid, wenn man die Flasche aus dem Kühlschrank holt, und öffnet?
(Außerhalb bestehen Standardbedingungen!)
Tip Antwort |
3. Aufgabe:
|
| Ein mit Gas gefüllter Gummiballon hat ein Volumen von 5 cm3 bei einer Temperatur von 15�C im Schatten. Durch
Sonneneinstrahlung erhitzt er sich auf 25�C und danach auf 30�C.
Um wieviel ist der Ballon bei 25�C bzw. bei 30�C größer als bei 15�C ?
Tip Antwort |
|
2. zu Reaktionstreibende Kräfte
|
| |